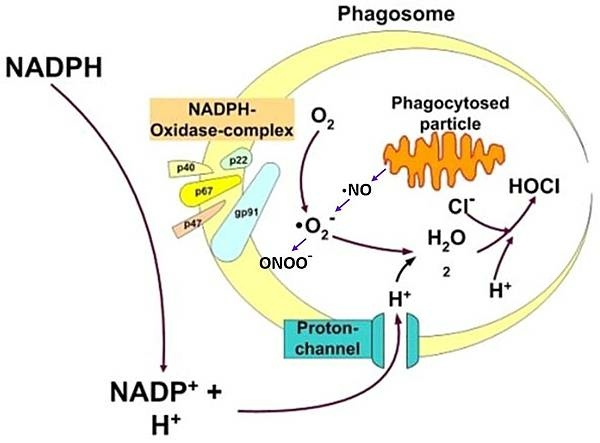
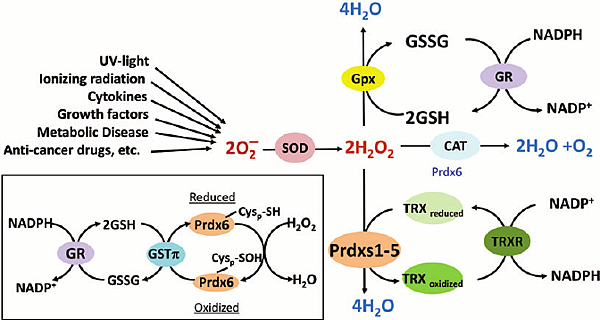
過去兩週發生疑似米酵菌酸(Bongkrekic acid,BA)中毒死亡的事件,以台灣醫療設備的現況,單純從食物中吃下一種化學分子引發敗血症(Sepsis-DIC)的機率極低,又不是吃多很多。這篇來回顧一下腸道免疫。
腸道主要菌種(Bacterial species)約300-500 species,每個Species有數十個不同的Genus--->數十個Family--->數十個Order--->數十個Class。一個人的腸道細菌含量約1014,正常情況下,它們所誘發的免疫反應(Cytokines)會刺激嬰兒腦神經發育,它們所產生的Short chain fatty acids有助於鞏固腸上皮黏膜組織。Bongkrekic acid是一種脂肪酸,如果你吃下一點米酵菌(Burkholderia gladioli),估計也很難在腸道佔有一席之地,產生微量的Bongkrekic acid也不至於造成疾病。
如果有一種細菌想在腸道定居,首先必須在數以兆計的現有細菌中競爭一席之地,然後不被腸道免疫弄死。
從1980年起,Interleukin從IL-1與IL-2,數字每年增加1-2兩個,1993有了新的變化,有一個cDNA叫CTLA-8從T cell hybridoma被篩選出來,其後被命名為IL-17,它會吸引Macrophage/Dendritic cell及Neutrophil至感染處引起發炎反應,也見於某些自體免疫疾病諸如 rheumatoid arthritis(類風濕性關節炎), psoriasis(乾癬), multiple sclerosis(多發性硬化),屬於Pro-inflammatory cytokine,但So what?Pro-inflammatory cytokines已經很多,包括IL-1, IL-6, IL-8, TNF-a, IFN-g等。
Th17觀念的建立要等到IL-23的發現(2000年),當時已知IL-23可促使已分化的Th1 cell分泌IFN-g。2003年IL-23偶然中被發現也可促使某種CD4+ T cell分泌IL-17,這種CD4+ T cell隨後被發現不同於已知的Th1與Th2,因而命名為Th17,主要分泌IL-17, IL-21, IL-22。
Th17的建立填補了Th1/Th2無法解釋的臨床現象,例如胃幽門桿菌(Helicobacter pylori, HP)感染,如果被感染的人無法清除幽門桿菌而啟動Th1/Th2 immunity,最後形成膿瘍,除了上腹不適之外,可能引起發燒或全身倦怠,但過了急性期之後,幽門桿菌引起的慢性胃炎常都沒有症狀,細菌一直與胃共生存在,免疫系統卻無法清除細菌,Th17的發現可解釋這一現象。
幽門桿菌接觸上皮細胞啟動TLR(Toll-like receptor)-LPS(Lipopolysaccharide) signaling,IL-1b自上皮細胞釋出,吸引Neutrophil及Macrophage過來吞食細菌,並分泌TNF-a及IFN-g等Cytokines,另外也包括IL-6及TGF-b(兩者都可經由上皮細胞及免疫細胞分泌),我們看看下圖:

iTreg是外來抗原誘發(Induced)的Treg;相較於T cell在Thymus發育時的Natural Treg(nTreg)。
如果免疫系統無法及時清除幽門桿菌,iTreg會壓制Th1及Th2的活性,使免疫反應轉向Th17,即Macrophage吞食幽門桿菌後將抗原訊息傳給Naïve CD4+ T cell。IL-1-b + IL-6 + TGF-b促使Naïve CD4+ T cell分化為Th17 cell,IL-23(來自感染處的Macrophage)再促使Th17 cell分泌IL-17, IL-21, IL-22如下圖:

IL-17 可吸引免疫細胞(Neutrophil/Macrophage/Dendritic cell/B cell/T cell)至感染處。
IL-21 促進Plasma cell分化及抗體分泌。
IL-22 刺激上皮細胞分泌抗菌蛋白(Anti-microbiial peptides)如Defensin。
新的細菌定居在腸道可用上面的觀念解釋,如果有Th1/Th2活化,會有短暫的腹部不適,如果該細菌沒有能力入侵上皮細胞,Th17自然形成。
-------
許多歷史文獻上的米酵菌酸中毒,可能的病因不在米酵菌酸,而在其它細菌的變異株產生的有機分子破壞某些人腸道的免疫系統,快速引發敗血症,尤其是Monocyte系列的免疫細胞(Macrophage與Dendritic cell)死亡,病人死亡速度非常快----->死亡與某種細菌的某種生化分子造成腸道Monocyte/Macrophage/Dendritical cell死亡(Necroptosis),T cell immumity失去Antigen presentation的活化,腸道免疫系統隨即崩潰,腸道細菌因而大舉入侵。缺乏免疫系統對細菌的局部化作用,整個腸道用凝血來包住細菌,阻擋細菌進入血液,最後耗盡血小板與凝血因子,這就是Sepsis-DIC(Disseminated intravascular coagulopathy)。
一個20幾歲的年輕人若發生肝膿瘍,培養出大腸桿菌,病因是這株大腸桿菌的某種蛋白(或其它分子)會促使這年輕人的Neutrophil走向死亡,但他的T cell immumity仍可將該株大腸桿菌局部化,因此只要使用最簡單的抗生素如Ampicillin,把細菌活動力減弱,Neutrophil就能再度發揮吞食細菌的功能。鼠疫桿菌會促使30-50%人的Monocyte/Macrophage死亡,情況就非常危急,因為T cell immunity會受到干擾,必須即時使用抗生素,否則感染一兩天,人就會死亡。
最進十年的免疫學研究,解釋數千年來,人類許多疾病的致病機轉。在現代醫療設備的支持下,單一的化合物中毒,病人可以撐很久不死,但免疫系統崩潰,發病兩天就能預知死亡趨勢。
wleemc 發表在 痞客邦 留言(74) 人氣(8,198)
 人體各系統的運作,最複雜的是神經系統,其次是免疫系統,兩者都有平衡機制來達成正常的功能。例如肢體運動包含來自三方面的神經支配才能維持動作的平衡與順利:
人體各系統的運作,最複雜的是神經系統,其次是免疫系統,兩者都有平衡機制來達成正常的功能。例如肢體運動包含來自三方面的神經支配才能維持動作的平衡與順利:
1. 用大腦皮質-視丘-脊髓的錐體徑路(Pyramidal tract)來發號施令。
2. 用錐體外徑路(Extrapyramidal tract)來調整(抑制)過強的發號施令。過強會出現僵硬,如巴金森氏症。
3. 用小腦來維持發號施令的精確性。小腦若失能,行走時會東倒西歪,無法依照大腦的意志往正確的角度行進,撿東西時手會對不準。
一個音樂家在演奏鋼琴入神時,他想到的只有樂譜,不會注意他的雙腳正踩著踏板。雙腳踩著踏板,沒有大腦的蓄意操控,是錐體外徑路的功能。他的手指能準確觸碰琴鍵是小腦的功能。
免疫系統有三大平衡,機轉都不清楚: Treg cell vs Neutrophil(Segment),如下面的病例: 78歲女性肝膿瘍的WBC-DC 免疫反應好的人,T cell immunity會將細菌局部化在肝臟的膿瘍部位,Treg cell抑制血中過多活化的Neutrophil(SEG)。T cell immunity發揮一次包圍細菌的功能,IL-2/IFN-g/TNF-a會活化Neutrophil一次,Treg cell會抑制一次Neutrophil,因此,血中的Neutrophil會上下波動,有時會出現正常的WBC-DC,例如6-25,WBC 5100, Seg 65.3%,有時WBC會被Treg cell壓過頭,例如7-20,WBC 2700, Seg 29.4%。如果Treg cell無法彈性壓制過多活化的Neutrophil,是一種免疫失衡,可能導致肺水腫或急性腎衰竭(Activated neutrophil釋出毒性物質對器官造成傷害)。 Treg cell vs CTL,如下面的急性B肝病例: 41歲女性,感染HBV,CTL攻擊被HBV感染的肝細胞,Anti-HBc IgM positive,因此是新的急性HBV感染,而非慢性B肝的急性發作。 CTL偵察到病毒入侵,會攻擊被感染的肝細胞(ALT/AST上升),接下來啟動T cell immunity。一般而言,CTL只是短暫攻擊肝細胞,ALT<500 U/L,病人只有輕微的身體不適,常會誤以為感冒,接下來T cell immunity對病毒進行局部化作用,Treg cell抑制CTL攻擊肝細胞,ALT/AST自動下降,90%以上的成人會在不知不覺中痊癒,HBV被Anti-viral cytokines(IFN-a/IFN-b)清除,約5-6個月產生Anti-HBs antibody。少數人Treg cell對CTL的抑制作用較差,CTL大量殺死被HBV感染的肝細胞,因而出現超高的ALT(此病人高達3522U/L)及黃疸(此病人Total bilirubin高達17.37 mg/dL)。這病人很幸運,CTL最終被Treg cell抑制下來,病毒被清除,並產生Anti-HBs antibody。如果CTL完全不受Treg cell抑制,將肝細胞完全摧毀(免疫失衡),就是猛爆性肝炎,需要換肝才能存活。 Treg cell vs B cell Treg cell會抑制B cell產生自體抗體,機轉不明。免疫失衡造成B cell產生自體抗體大致可分為三種方式: 1.Natural antibody可與死亡的細胞殘骸蛋白、脂質、醣基、DNA做微弱的結合,然後殘骸被Macrophage清除。製造Natural antibody的B1a cell不會進入Germinal center進行Somatic hypermutation,但在某些人會發生例外,即B1a cell進入Germinal center進行Somatic hypermutation,原本與細胞殘骸蛋白、脂質、醣基、DNA做微弱的結合的抗體變強了,於是產生Autoantibody against nuclear/cytosolic/plasma membrane proteins、Phospholipid、DNA。當測到High titer anti-nuclear antibody時,代表Treg cell vs B cell發生免疫失衡,最典型的病例是全身性紅斑狼瘡,血中可測到數十種Autoantibody。 2.IgG4上升也是Treg cell vs B cell發生免疫失衡,使產生Autoantibody的B cell浮現出來,機轉十分複雜且難懂,請參考下文: https://wleemc.pixnet.net/blog/post/121509768 IgG4上升也可能附帶造成Treg cell vs CTL失衡,導致CTL對癌細胞的監控能力變差,因此IgG4上升與癌症發生率成正相關。 3.B cell經由Molecular mimicry(分子相似)產生Autoantibody(an antibody against a foreign antigen as well as a self-antigen),現在臨床上常見的病例如下: i)胃幽門螺旋桿菌(Helicobacter pylori, HP)慢性感染,Anti-HP antibody可能對抗血小板,造成Immune thrombocytopenia(ITP),約有40%的ITP與HP感染有關。 ii)黴漿菌(Mycoplasma pneumoniae,MP)感染,anti-MP antibody可能對抗紅血球,造成溶血性貧血。anti-MP antibody,也可能對抗血小板,造成ITP。 iii)某些病毒(流感、EBV、CMV)感染後,B cell產生的抗病毒抗體對抗神經膠細胞的Ganglioside,引發Guillain-Barre syndrome。值得注意的是,所有的疫苗都可能引發Guillain-Barre syndrome。 外來抗原進入人體可能經由Autoimmune CTL或B cell引發各種自體免疫疾病。如何降低自體免疫疾病發生的機率?跟國家防衛一樣,決戰於境外,殲敵於灘頭,身體稍有不適,先吃兩次N+E再觀察後續症狀。把外來抗原往自己身上打是愚蠢的行為。wleemc 發表在 痞客邦 留言(38) 人氣(5,081)
巴金氏症的研究在1997年發現alpha-synuclein(aSyn)在腦部發生異常聚集,2003年Heiko Braak在巴金森氏症病人的屍體解剖發現aSyn在迷走神經的主幹聚集,因此假設(Braak's hypothesis)認為腸道微生物引起的慢性發炎反應,導致某種微生物的分子X(蛋白、醣基、脂質等)促使人體內生性Prion或Prion-like protein(PrLP)無法形成正常結構(Misfolded)而在腸道細胞發生異常聚集。2016年這項假設被證實存在:
http://www.cell.com/fulltext/S0092-8674(16)31590-2
1. 在實驗室製造一種老鼠可大量產生aSyn,aSyn過多就會在黑質(Substantia nigra)異常聚集,當然也會在其他神經細胞聚集,但老鼠壽命短,在黑質聚集較快,因此很快就會引發巴金森氏症。
2. 如果把aSyn過多的老鼠養在無菌環境下,症狀會較輕,代表巴金森氏症延遲出現。巴金森氏症「病鼠」的腸道細菌會加快加重 「無菌鼠」巴金森氏症的病程。

腸道免疫反應 + 腸道微生物的分子X促使腸道細胞aSyn misfolded而聚集,蔓延至迷走神經細胞的aSyn,鏈鎖聚集上傳至腦部,破壞Basal ganglia的黑質,導致巴金森氏症。
60歲以上,約有1%的人會有輕重不一的巴金森氏症。為何99%的人沒有?可能與免疫細胞阻止分子X潛入腸道上皮細胞,及人體有對抗aSyn聚集的機制。
Braak's hypothesis已有20年歷史,因此只要有一種蛋白製劑打進人體,就會有人去檢視它是否是Prion or Prion-like protein。新冠疫苗在大規模注射前就有人預測Spike protein是Prion-like protein,於是立刻有人證實Spike protein可促使Tau protein聚集(阿茲海默症的病因之一)。
https://www.nature.com/articles/s41467-021-25855-2
Spike protein促使aSyn聚集的研究也在2022年發表於Pubmed:
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8949667/
wleemc 發表在 痞客邦 留言(24) 人氣(3,055)
wleemc 發表在 痞客邦 留言(36) 人氣(3,609)
細菌的蛋白種類約2000-6000,例如大腸桿菌約4600種蛋白,不像病毒只有數十種,因此人類的T cell幾乎都能辨識細菌的蛋白為Non-self antigen而活化。當細菌感染時,T cell immunity都能對細菌進行局部化的包圍作用,接下來如果Neutrophil能進入包圍圈吞食細菌,感染(疾病)就不會發生。
下圖是Neutrophil對抗細菌的運作:

https://onlinelibrary.wiley.com/doi/full/10.1002/advs.202306457
1. Neutrophil是短命的細胞,正常情況下,壽命只有8-12小時即走向Apoptosis (Non-inflammatory)。
2. 細菌感染時(Inflammatory),Neutrophil經由Pyroptosis釋出IL-b,吸引其它免疫細胞過來;形成NETs(Neutrophil extracellular traps)網住細菌,以利其它Neutrophil吞食細菌;經由Ferroptosis釋出Oxidants,有如毒氣,降低細菌的活力;感染處少量的Neutrophil走向Necroptosis釋出DAMPs(danger-associated molecular patterns)可活化Innate immunity。
3. Necroptosis原本是用來調節血中經Cytokines(TNF-a, IFN-g)活化的Neutrophil的量,防止血中過多活化的Neutrophil釋出Oxidants及Protease對器官造成傷害,但細菌的蛋白會利用這個Neutrophil的死亡訊息,讓感染處被T cell immunity局部化的Neutrophil失去吞食細菌的能力。下面的病例是特殊細菌對Neutrophil發動猛烈的Necroptosis,該細菌得以不斷產生Protease突破T cell immunity的包圍圈(Collagen fiber),感染處的Neutrophil毫無招架之力,快速走向Necroptosis。如果感染範圍尚小時,立刻服用抗生素降低細菌的活力,可免除被截肢的悲慘結局。
溫哥華消防局(Vancouver Fire Rescue Services)助理局長Christopher Won與妻子Marie Hui一家四口在東南亞旅遊期間,疑在新加坡時感染「食肉菌」,引致壞死性筋膜炎,未知是如何感染。他其後來到香港,因病情惡化求醫,醫院為他截去右小腿保命。
https://www.hk01.com/article/994638?utm_source=01articlecopy&utm_medium=referral
所謂的食肉菌可能是下面幾種細菌遇上適合的人的Neutrophil,使Neutrophil加速走向Necroptosis,防止細菌被Neutrophil吞食:
Staphylococcus aureus
Streptococcus viridans
Streptococcus pyogenes
Vibrio vulnificus
Clostridium perfringens
下面是台灣的病例,及時使用抗生素,得以免除截肢的命運。
https://reurl.cc/aLg9M9
某種細菌遇上某個人的Neutrophil,經由TNF-a + Type I IFN(IFN-a,IFN-b) + Bacterial proteins,即可能促使感染處的Neutrophil加速走向Necroptosis。
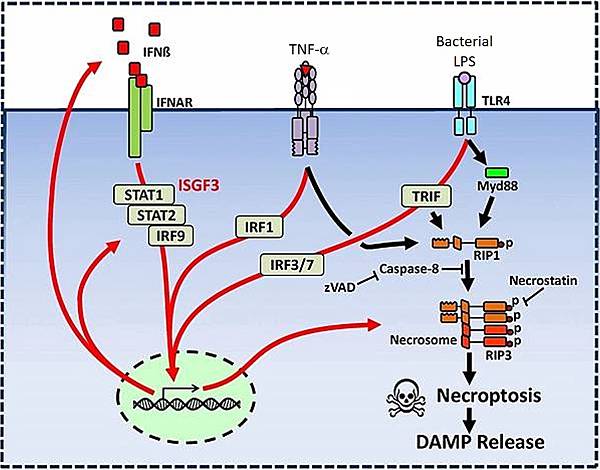
https://www.pnas.org/doi/10.1073/pnas.1407068111
下面的病例也可能是Neisseria meningitidis遇上一個健康軍人的Neutrophil引發Necroptosis,未及時服用抗生素造成的不幸。
20歲的張姓士兵為志願役一兵,服役1年許,21日下午6點休假離營,原定23日24時收假,但22日因身體不適由家人陪同至桃園國軍總醫院就醫,未料病情突惡化,於23日不治身亡。 https://www.chinatimes.com/newspapers/20170727000405-260118?chdtv wleemc 發表在 痞客邦 留言(75) 人氣(4,573)
CBC(Complete blood count) 是診斷疾病的Routine,但極少醫師有能力正確判讀CBC。正常人的Neutrophil壽命約8-12小時(很短命),因為Neutrophil胞膜上的Fas比其它細胞多,血中有Fas ligand(FasL),會促使Neutrophil走向Fas-FasL-mediated apoptosis (death signal)。當Neutrophil吞食細菌後會分泌TNF- a ,作用在Neutrophil胞膜上的TNF receptor,會傳遞Survival signal,當Survival signal > Death signal,原本短命的Neutrophil壽命就會延長至數天。下面是細菌感染時,CBC-DC的經典變化:
25歲男性,主訴腹瀉兩天。

6月5日WBC 11400/ul,Neutrpohil(Seg) 83.2%。這是Survival signal > Death signal造成Neutrophil壽命延長,大量累積在血中被測到。
6月7日WBC 3900/ul,Neutrpohil(Seg) 63%。Neutrophil被TNF-a 活化後不會無節制停留在血中,在細菌性腸炎,活化的Neutrophil會在腸炎處聚集,血中過多的Neutrophil會走向Necroptosis(血中Neutrophil若持續2-3倍高於正常值,可能引發急性腎衰竭或肺積水造成呼吸衰竭),這是免疫系統清除過多的免疫細胞的平衡機制,避免過多活化的Neutrophil對器官造成傷害。
6月11日WBC 6200/ul,Neutrpohil(Seg) 63.6%。造成腸炎的細菌被T cell immunity局部化,血中TNF- a 恢復正常,此時Fas-FasL-mediated apoptosis > TNF-a/TNF receptor-mediated survival,WBC回到他的常態(WBC 6200,Seg 63.6%)。 細菌感染時的WBC-DC千變萬化,如上例WBC從11400降至3900時,抽血可能抽到正常的WBC-Neutrophil,如下面的病例: 39歲男性,主訴右上腹痛兩天。 WBC 7500, Neu. 70.7%,但CRP 5.09 mg/dL (正常小於0.1 mg/dL) 也可能剛好抽到Neutrophil發生Necroptosis時的低值,如下面的病例: 35歲女性,主訴早晨起床時有點噁心,吃不下東西。 WBC 3400, SEG 50.1%,CRP 4.25 mg/dL ----------------- Neutrophil的胞膜上Fas多,老化死亡是經由Type I apoptosis,即Fas/FasL-mediated apoptosis。上皮細胞的胞膜上Fas較少,老化死亡是經由Type II apoptosis,即細胞膜上的Receptor tyrosine kinase(RTK)變少,RTK/PI3-K/Akt/mTOR survival signal變弱,於是Caspase-8 death signal > PI3-K/Akt/mTOR survival signal,細胞走向t-Bid/Cytochrome c-mediated apoptosis。 wleemc 發表在 痞客邦 留言(34) 人氣(2,671)
黑死病在中世紀造成歐洲近半數人口死亡,病因是鼠疫桿菌(Yersinia pestis)
。中國歷史上,南宋亡於蒙古,明朝亡於女真,都與當時鼠疫大流行有關。1880-1950年流行於中國東北與西南的鼠疫,蔓延至印度及東南亞,單在印度和中國,就有超過1200萬人死亡。二戰以後,抗生素廣泛使用,在我們有記憶的年代,病毒對人類的威脅遠大於細菌,本篇來探討這個問題。
1990年以後T cell receptor(TCR)與Major Histocompatibility complex(MHC)的配對研究清楚之後,許多免疫學的矛盾一一被釐清。MHC-I表現在人體所有細胞的胞膜上,CTL用TCR來辨識被病毒或細菌感染的細胞經由MHC-I呈現出來的Peptide為外來抗原。MHC-II只表現在APC(Antigen-presenting cell,包括Dendritic cell、Macrophage、B cell)的胞膜上,Th cell用TCR來辨識APC經由MHC-II呈現出來的Peptide為外來抗原。TCR與MHC之間只有九個胺基酸做為接合點。

圖一:TCR與MHC-II的立體結構關係。

圖二:TCR與MHC-II九個胺基酸的接合點範例,第3號胺基酸懸空,未與TCR及MHC接觸。
細菌與病毒對人類的威脅程度差異在兩者的基因數(細菌>>>病毒)。細菌的基因少則600多個(如黴漿菌),多則四五千個(大腸桿菌約4500多個),人類的T cell幾乎都可以辨識細菌龐大數量的蛋白為外來抗原(Non-self antigen)而活化,並將致病細菌局部化。二戰以後,病毒對人類的威脅大於細菌,是因為病毒基因數少,例如新冠病毒只有29個蛋白,因此一定有少數人的TCR無法辨識這29個蛋白被細胞分解後用MCH呈現出來的Peptide為Non-self antigen。如果CTL無法辨識,就無法在鼻咽喉偵察到病毒入侵,如果Th cell也完全無法辨識,那麼即使二十幾歲健康的年輕人,打過兩三劑新冠疫苗,染疫必遭天擇淘汰,沒有解藥。
鼠疫是細菌感染,人類的T cell immunity一定能將鼠疫桿菌局部化(例外極少),二戰以前,鼠疫之所以可怕,是因為鼠疫桿菌的蛋白會對免疫細胞誘發不可逆的Necroptosis(因人而異)。
Necroptosis of infiltrated macrophages drives Yersinia pestis dispersal within buboes
https://pubmed.ncbi.nlm.nih.gov/30232285/
抗生素改變鼠疫的命運,臨床上實證,只要用抗生素弱化細菌的活性,就能逆轉細菌蛋白對免疫細胞造成的Necroptosis,Macrophage與Neutorphil就能反擊孱弱的鼠疫桿菌。
圖三:Cell survival vs Apoptosis vs Necroptosis
TNF-
a與Type I interferon(IFN-
a與IFN-
b)是發炎反應的重要Cytokines,兩者對免疫細胞行使正常功能扮演重要的角色。TNF-
a對免疫細胞傳遞Survival signal,可活化所有的免疫細胞。Type I IFN可促使被病毒或細菌感染的細胞大量表現MHC-I,並促使APC大量表現MHC-II。
Type I IFN也是Anti-viral cytokines。在某些情況下,
TNF-a與Type I IFN協力作用,會促使免疫細胞加速死亡(Necroptosis),而非正常情況下的老化凋亡(Apoptosis)。
Apoptosis與Necroptosis是免疫系統維持一定數量細胞的恆定機制。例如一次流感造成咽喉有淋巴球聚集(T cell immunity對病毒的局部化作用),當病毒被清除後,聚集的淋巴球會就地死亡(Necroptosis),咽喉腫痛因而消失。在某些情況、發生在某些人身上,病毒或細菌的蛋白可能運用此機制來抑制免疫細胞行使正常功能(TNF-a + Type I IFN + Viral or bacterial proteins X+Y+Z ---->Necroptosis of immune cells),讓Monocyte/Macrophage/Neutrophil誤入Necroptosis pathway。
「感染」生病其實是常態下「不感染」的例外,比方說肝膿瘍正常不會發生,因為在膿瘍發生前,細菌就被Neutrophil偵察到,並啟動T cell immunity對細菌進行包圍作用,Neutorphil與Macrophage在膿瘍發生之前就進入包圍圈內清除細菌,這是常態。如果細菌的蛋白對Neutrophil造成Necroptosis(這是例外,且因人而異),T cell immunity仍可對細菌進行包圍作用,但Neutrophil無法進入包圍圈內清除細菌,細菌就會分泌酵素分解包圍圈的Collagen fiber,T cell immunity再對細菌進行另一波包圍,這樣包圍-分解-包圍-分解-------持續進行,膿瘍就越養越大,發燒就醫時用超音波才發現肝臟有一個膿瘍。抗生素發現後,細菌感染不再對人類造成重大威脅,但T cell immunity必須先把細菌感染局部化,否則抗生素會沒效,例如八十歲的老人感染細菌性肺炎,T cell immunity功能不良,無法把細菌完全局部化,用再強的抗生素都沒用。

圖四:肝膿瘍發生時,T cell immunity對細菌的局部化作用正常,但Neutrophil受細菌蛋白的影響,誤入Necroptosis pathway,因此儘管細菌已經被T cell immunity包圍,Neutrophil卻無法正常清除細菌,於是細菌不斷分泌酵素分解包圍圈的Collagen fiber,膿瘍就越養越大。
登革熱病毒會引發Monocyte走向Necroptosis,如果Necroptosis是可逆的,發病後自然會痊癒,不用吃藥,也沒藥可吃;如果Necroptosis是不可逆的,病人必因出血性登革熱而死亡,沒有解藥。 wleemc 發表在 痞客邦 留言(117) 人氣(5,500)
打過新冠疫苗後,抗體怎樣生出來?
Naïve B cell-IgM在疫苗注射處抓到抗原(Spike protein)之後,如果IgM-Spike protein結合夠緊,Naïve B cell就會活化,回到局部淋巴結(主要在腋下、頸部,但疫苗抗原會經由血液循環全身)進行細胞分裂,然後產生抗體IgM,但單靠Naïve B cell活化產生的抗體僅曇花一現,很快就後繼無力,所產生的抗體抽血也測不到,這種Naïve B cell短暫活化之後,將迅速恢復平靜。
Naïve B cell-IgM抓到Spike protein後,需要Th cell也被Spike protein活化,分泌十幾種Cytokines,該Naïve B cell才會進一步分化、快速分裂,並進行Class switch,製造所需求的抗體。下文Table 1顯示各種Cytokine對B cell分化、分裂、Class switch的影響:
https://www.frontiersin.org/articles/10.3389/fimmu.2014.00065/full
Table 1值得注意的是,某些病毒蛋白會促使IgM-->IgE(需要IL-4、IL-13、IL-21),引發蕁麻疹。IL-12、IFN- a 、IFN- g 、TGF- b 可抑制IgE產生。注射疫苗或病毒感染是否引發蕁麻疹,因人而異。但麻疹與水痘是病毒先感染上呼吸道,再經由上呼吸道分泌物中的大量病毒感染皮膚上皮細胞。
疫苗注射後,B cell產生大量抗體若能在血中被測到,需要Th cell(CD4+ T cell)協助。Dendritic cell(DC)在疫苗注射處吞食外來抗原(Spike protein),回到腋下及頸部淋巴結,將疫苗抗原分解成九個胺基酸的Peptide,讓T cell receptor(TCR)辨識出Non-self antigen而活化,如下圖:

圖一: Activated DC與CD4+ T cell(Th cell)進行Antigen presentation,將外來抗原的訊息傳遞給Th cell。
Naïve Th cell活化後會分化成Th1、Th2、Treg、Tfh(follicular helper T cell)。Naïve B cell-IgM抓到病毒蛋白後,若要進一步分化產生大量抗體,需要Th1與Th2分泌Cytokines幫忙,如下圖:
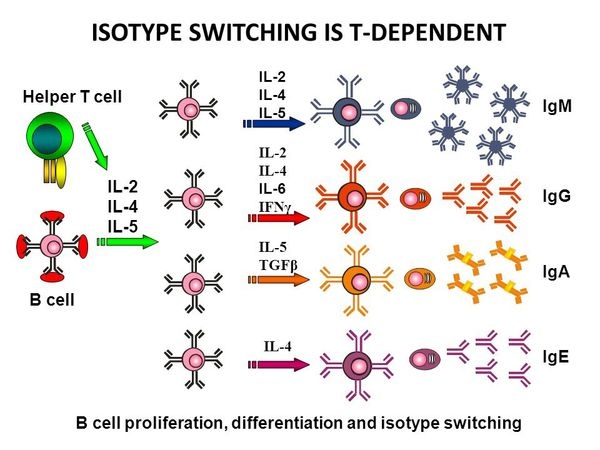
wleemc 發表在 痞客邦 留言(71) 人氣(4,389)
醫學院免疫學老師出考題只會出他懂的,他不懂的,不會教,也不會考,考試沒考的反而是最重要的。T cell immunity最後收網要靠Fibroblast,不但對抗細菌與病毒是如此,對抗癌細胞也是如此。幾乎沒有教免疫學的老師或教病理學的老師講出發炎組織及腫瘤組織切片中的Fibroblast的重要性,醫學生甚至不曾在顯微鏡下多看它們一眼。
我問過大五大六醫學生或PGY,為何腫瘤都是硬塊?問過數十次,沒有人知道是「T cell immunity與Fibroblast經年累月圍攻癌細胞造成」;如果這樣能把癌細胞逼死,就不會有癌症發生。如果某個癌細胞在Autophagy(自噬作用)艱困的環境中活了下來,一次又一次掙脫T cell immunity與Fibroblast的圍攻,這株癌細胞就被篩選出來繼續坐大。

https://librepathology.org/wiki/Invasive_ductal_carcinoma_of_the_breast
原位乳癌病理切片(Ductal invasive carcinoma in situ)
綠箭頭標示淋巴細胞,主要是T cell。
紅箭頭標示纖維母細胞(Fibroblast)或間葉細胞(Mesenchymal cell),間葉細胞可分化成纖維母細胞(圖中狹長梭形的細胞)。Fibroblast被免疫細胞吸引至腫瘤附近分泌纖維蛋白(上圖細胞間的粉紅色),並將腫瘤細胞困在纖維結締組織中,使之缺乏養分供應而死亡,如圖中的黑箭頭,一群乳癌細胞被纖維組織包圍;「Dead」可能是缺乏養分供應而死亡的癌細胞。乳癌會形成硬塊,是某個癌細胞在缺乏養分供應的艱困環境下利用Autophagy活了下來,一次又一次掙脫T cell immunity與Fibroblast的圍攻,這株癌細胞就被篩選出來繼續坐大。 新生兒也有T cell,但T cell receptor(TCR)尚未進行基因重組,對外來抗原的辨識作用跟NK cell(Natural killer cell)差不多,因此對外來抗原的局部化作用很差,遇上致病病毒或細菌,若現存於新生兒體內的T cell無法將致病細菌或病毒局部化,新生兒就會死亡。新生兒的IgM-B cell也沒有經過抗體的基因重組,因此母親從胎盤輸給胎兒的IgG就非常重要。新生兒對抗致病病毒或細菌的三種方式如下: 1. 從母親獲得的IgG與細菌或病毒結合,然後被Macrophage、Monocyte或Neutrophil吞食-分解。 2. 用NK cell去發現被病毒感染的細胞,然後把細胞殺死,一併殺死病毒。 3. 試著用現存於體內的T cell對細菌或病毒進行局部化作用。 如果以上三項都無法阻擋細菌或病毒入侵,新生兒會遭天擇淘汰,因此,新生兒呱呱墜地之後要立刻進行抗體基因重組(產生種類繁多而複雜的抗體來取代母親給他的IgG)及T cell receptor(TCR)基因重組(產生種類繁多而複雜的TCR來辨識入侵的細菌或病毒為Non-self antigen)。 B cell progenitor在骨髓進行抗體基因重組最旺盛的時期是新生兒出生六個月之內,至此,B cell clone基本上已定型,Clone number可達1011,所產生的抗體足以取代母親從胎盤傳給新生兒的IgG。一歲以後至老死,不管產生多少新的B cell clones,都是上述1011的零頭。 新生兒出生後至3歲,T cell receptor會快速進行基因重組,大部分的人到三歲時,Naive T cell (Th與Tc) clone number已定型(>107,可達108),但仍會改變,到六歲時差不多就快停了。因此上小學之後打疫苗是「弊大於利」,至於打或不打,請自行決定,不要一直來問版主,版主不對任何人負責。青春期過後,99.99999%的人不會產新的Th(Helper T cell)與Tc(Cytotoxic T cell),此後打疫苗完全沒用。 T cell對膿瘍細菌的局部化作用如下圖病理切片: https://webpath.med.utah.edu/CINJHTML/CINJ021.html B cell progenitor在骨髓終身可進行抗體基因重組產生新的B cell clone (X)。淋巴組織中「與生俱來(來自上述1011)」的Follicular B cell可經由局部感染進入經由T cell活化而形成的Germinal center進行Somatic hypermutation,產生新的B cell clones(Y)。以上兩種方式所產生的新B cell clone製造出來的抗體與該次感染清除細菌或病毒的關係不大。值得注意的是,必須有T cell活化才能促使骨髓的B cell progenitor cell進行基因重組;必須有T cell 活化,淋巴組織的Germinal center才會形成。上圖T cell對細菌的局部化作用不需要新的B cell clone(X與Y)來產生專一性抗體,圖中那一圈就是T cell immunity與Fibroblast的傑作,若沒有那道長城,細菌早就擴散出去引發敗血症。 T cell對新冠肺炎的局部化作用如下圖,上(胸部X光片),下(電腦斷層): https://erj.ersjournals.com/content/early/2021/02/04/13993003.04188-2020 上圖T cell對細菌的局部化作用不需要新的B cell clone(X與Y)來產生專一性抗體。局部化良好的新冠肺炎,代表CTL沒在鼻咽喉及氣管/支氣管發現病毒入侵(偵察及攔截作用失靈,但Th cell在肺臟能快速辨識新冠病毒的蛋白為Non-self antigen,及早起啟動T cell immunity/fibroblast/collagen fiber對病毒的包圍作用。如果Th cell完全無法辨識病毒為Non-self antigen,兩側肺臟會在發病之後迅速變白,即使20-40歲的健康壯男得流感也會慘遭天擇淘汰。打疫苗無法改變天擇。https://udn.com/news/story/7266/7662655https://health.ltn.com.tw/article/breakingnews/4560769 wleemc 發表在 痞客邦 留言(238) 人氣(8,397)
版主打算寫幾篇文章來回顧一下免疫學,下面有兩篇頂級期刊的Review article:
Understanding T cell responses to COVID-19 is essential for informing public health strategies (Science Immunology)
https://www.science.org/doi/10.1126/sciimmunol.abo1303
The T cell immune response against SARS-CoV-2 (Nature Immunology)
https://www.nature.com/articles/s41590-021-01122-w
讀過版主的免疫學,再去讀這兩篇發表在頂級期刊的文章,會有一種「不知所云」的感覺。如果你寫e-mail給上面兩文的作者,問他「What is T cell immune response?」他的回答仍會讓你感覺「不知所云」,而且矛盾重重。版主用一句話就能讓沒學過免疫學的人知道「What is T cell immune response?」一言以蔽之,「T cell immune response就是將外來抗原局部化,防止其擴散」這麼簡單。 遍尋Pubmed,你幾乎找不到免疫學專家把T cell immune response解釋清楚。版主1984年二月第一次修免疫學,讀過兩本免疫學原文書,同樣不知所云,當時讀不懂的原因在T cell receptor(TCR)仍只是一種假設的存在,1984年T cell receptor(TCR)的cDNA才被篩選出來。 https://www.nature.com/articles/308145a0 1990年以後,TCR與MHC(Major histocompatibility)的關係逐漸被確立,1996年TCR-MHC Antigen presentation正式寫入免疫學教科書(Janeway Immunobiology 第二版)。1996年諾貝爾醫學獎得主即研究「MHC restriction of TCR」。 1996年我在美國唸書時再修一次免疫學,美國的教授真的比較了解「T cell immune response 」嗎?「No,他們講到Th1、Th2的作用blablabla,你再問,他們就講不下去了!」
高中時期因為對醫學有莫名的憧憬,1982年我在中國牙與國防醫選擇了國防醫。如果我沒在陸軍官校結識我的班長,我可能寫不出「T cell immune response就是將外來抗原局部化,防止其擴散」這個簡單的結論。 1984年一月我忙著準備期末考,實在沒時間去考慮軍事學那幾十個反攻大陸在戰場上遇到的狀況,山川、地形、河流都不在台灣。我記得教官講了一句現在聽起來很可笑的話:「反攻大陸時軍醫要在戰場後方設置野戰醫院,一個野戰醫院是一個營的編制,你們要想像怎樣領導一個營作戰。」考前我把班長從部隊請來台大附近的一家餐廳,在那兒我把所有的戰場狀況丟給他,請他幫我解決。好老師的一堂課勝過你讀十年書,原來所有的戰爭都是在「偵察、攔截、包圍、殲滅」中鬥智。 我讀醫學系是那種把原文書當英文讀本來唸的學生,在三總實習時,我很快就發現三總主治是不學無術的低能,我無法在裡面生存。1995年我與國防醫學院院長鬥了一場之後退伍,赫然發現美國哥倫比亞博士的水平不過如此而已。看過軍醫局局長與國防醫學院長那副嘴臉(跟現在的柯文哲差不多),退伍後,我的人生目標很清楚,美國大學哲學博士--->醫學中心主治--->部定教授,到此為止,其它一概拒絕,包括疫情期間所有媒體的訪問及演講邀約。 我在美國把Janeway Immunobiology當英文讀本唸完後,終於從紙上談兵的戰場上得到下面的結論: 1.CTL只負責偵察病毒入侵,不能濫殺細胞。 2.Th cell活化後會對病毒進行攔截與包圍的作用。 3.Treg cell會抑制CTL毒殺被病毒感染的細胞。 4.T cell immune response最後會擴大Anti-viral cytokine的分泌,殲滅病毒。 5.中和抗體對清除病毒沒有存在的必要。若沒有抗病毒的T cell immune response,中和抗體濃度再高也沒用,感染必遭天擇。 wleemc 發表在 痞客邦 留言(58) 人氣(4,220)