代謝是複雜的生化反應,Glucose如何進入細胞是一門大學問,Fatty acid進入細胞又是另一門大學問。這篇文章的問題是:Insulin resistance是甚麼?
醫學生常會有一個籠統的答案:人體細胞對Insulin感應差,因此Glucose無法進入細胞進行氧化。
其實,Glucose進入細胞不需要Insulin,但人體不能沒有Insulin。Glucose transporter (Glut)的研究改變醫學對血糖代謝的觀念,Glut1與Glut3存在於各種細胞的胞膜上,Glut1最多的細胞是紅血球,Glut3最多的地方是神經細胞。當你吃過飯後,血中的Glucose會經由Glut1與Glut3進入細胞,提供細胞能量來源。當細胞需要Glucose時,Glut1與Glut3蛋白的製造會增加,位於細胞膜上的Glut1與Glut3 channel也會打開,下圖顯示Glut1與Glut3的複雜調控。
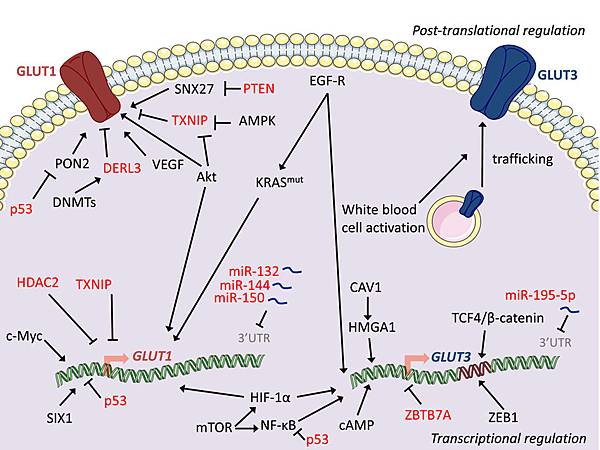
圖一: GLUT1 的調控在Tracriptional (gene) 及 Post-translational (protein) 兩個層面, GLUT3的調控主要在Transcriptional level.
https://febs.onlinelibrary.wiley.com/doi/10.1111/febs.14577
因此你體內一天沒有Insulin,日子仍會過得好好的,一個月沒有Insulin,如果你正在減肥,你會驚訝這個月減肥效果驚人,一口氣瘦了15公斤。你減肥成功很得意,但身旁關心你的朋友可能會建議你去看醫生,檢查一下是否得了癌症。這是Type 1 DM(第一型糖尿病),胰臟 islet b-cell 突然受T cell或自體抗體攻擊而全部死亡,偶而在門診遇到異常體重減輕的人,一測血糖超過500mg/dL。
為何初期Type 1 DM,異常體重減輕,卻可能沒有任何症狀?細胞沒有Glucose可用,難道會沒事嗎?其實Glut1與Glut3不受Insulin影響,細胞若需要Glucose,Glucose可從Glut1與Glut3進入全身細胞,因此Type 1 DM病人的細胞並不缺Glucose。Insulin的功能並非促使Glucose進入腦心肝肺腎等人體重要器官,而是促使Glucose經由Glut4進入骨骼肌與脂肪組織,轉變成肝醣(主要在骨骼肌)及脂肪酸(主要在脂肪組織)。

圖二: Glut4存在骨骼肌及脂肪細胞的Cytosol,當有Insulin/Insulin receptor signaling時,Glut4轉移至Cell membrane,促使Glucose進入骨骼肌及脂肪細胞。
Insulin另一重要功能是「促進肝醣合成」及「抑制脂肪水解」。如果沒有Insulin,脂肪組織會自動水解,Glucose無法有效率地合成肝醣,當骨骼肌缺乏肝醣時,便會直接氧化脂肪酸(Insulin使Fatty acid成為備用燃料,當人體缺少Insulin,細胞會直接氧化Fatty acid)。臨床上常見Type 1 DM的病人,除了體重驟減之外,身體不覺得有何不舒服,直到長期脂肪酸氧化導致「酮酸」累積太多才突然出現症狀。在我行醫生涯中遇過至少五位50歲以下的年輕榮民,當年服役出現酮酸中毒時,感覺全身倦怠無力,以為只是感冒,結果都是早點名沒出現,昏睡在床,送醫院才發現是Diabetic ketoacidosis。
我們再來談Insulin resistance。沒有Insulin,並不妨礙細胞使用Glucose做為能量來源,所以Insulin resistance 只是針對脂肪組織及骨骼肌的Glut4無法感受Insulin的刺激,血中多餘的Glucose無法順利進入骨骼肌合成肝醣(Glycogen)或進入脂肪組織合成脂肪酸(Fatty acid)。高血糖狀態下,當細胞拿到足夠的Glucose後,便不會再從血中接收Glucose (可以視作Glut1/Glut3 resistance),剩下的Glucose原本要轉變成肝醣及脂肪,但脂肪組織儲存脂肪及骨骼肌儲存肝醣及脂肪的空間早就已經滿了,於是就會拒絕Insulin/Insulin receptor signaling,即Glut4停留在Cytosol,沒有轉移至脂肪組織及骨骼肌的細胞膜。
正常人吃完飯後Glut1/Glut3會將Glucose自動帶進細胞,需要多少就帶進多少,滿足之後,Glut1/Glut3便會關閉。多餘的Glucose一方面靠Glut2進入肝臟,用於合成肝醣,然而最終維持飯後血糖低於140 mg/dL及禁食12小時血糖低於100 mg/dL,則是靠Glut4回收血中過多的Glucose至骨骼肌及脂肪組織。
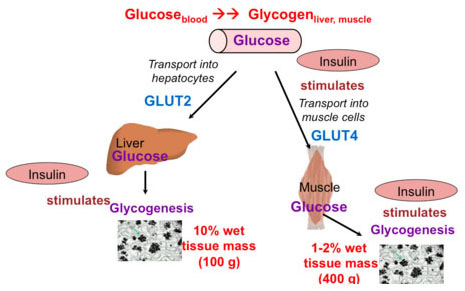
圖三: 飯後Glucose經由Glut2進入肝臟合成人體20%的肝醣,然而大部分的Glucose要經由Insulin/Insulin receptor signaling使Glut4發揮最大的功能,把Glucose送至骨骼肌合成人體80%的肝醣。
Glucose轉變成肝糖儲存於肝臟及骨骼肌,如果還有剩下,便會經由Glut4送至Adiopocyte氧化成Acetyl-CoA --->Fatty acid儲存在脂肪組織,當脂肪組織的儲存空間被佔滿後,肝臟便成為儲存脂肪的地方。因此,Insulin resistance發生前,常伴隨嚴重的脂肪肝及血脂異常,原因是當肝臟的脂肪儲存達到無法負荷過多的Glucose自Glut2進入肝臟時,用於合成Fatty acid的Acetyl-CoA便會用來合成Cholesterol---->Bile salt,自膽汁排出去。最終的結果,除了Insulin resistance之外,肝臟合成過多的Cholesterol導致血中LDL增加。
Type 2 DM病人為何會有「想吃」的症狀?是細胞缺少Glucose嗎?不是!是因為飯後兩小時血糖大於140 mg/dL仍不足以促使b-cell分泌更多的Insulin,因此需要進食使血糖飆高去促使更多更多的Insulin讓Glucose進入骨骼肌與脂肪組織,如此便形成一個惡性循環。
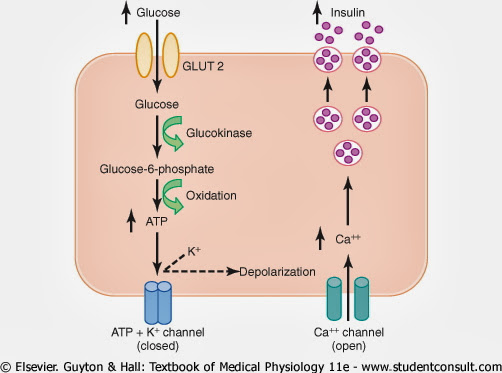
圖四: 是醫學生必須知道的Insulin分泌機轉。b-cell胞膜上的Glut2可讓Glucose自由進入(一如肝臟),進入b-cell的Glucose越多,Insulin的分泌就越多。
關於Glucose的代謝,Glut 屬於SLC2 family transporter,在各器官的的分布十分複雜,簡單的記憶如下:
1) Glut1 與 Glut3 廣泛分布於各種細胞,細胞需要Glucose時,Channel便會打開。
2) Glut2 分布在b-cell及肝臟,對Glucose進入b-cell及肝細胞沒有嚴格的管控。
3) Glut4 分布在骨骼肌、心肌及脂肪組織,受Insulin調控,維持飯後兩小時血糖小於140 mg/dL,空腹12小時血糖小於100 mg/dL。Insulin resistance 其實就是骨骼肌與脂肪細胞儲存脂肪的空間已滿,Glut4拒絕Insulin/Insulin receptor signaling,血中過多的Glucose無法被骨骼肌與脂肪細胞回收轉變成脂肪儲存起來。
- Aug 30 Sun 2020 11:10
生化-代謝-2(Insulin resistance)
close
全站熱搜
 留言列表
留言列表
發表留言



 留言列表
留言列表
 {{ article.title }}
{{ article.title }}