病理課本Neoplasm章節寫:Of interest, when RAS mutations are present in a tumor, activating mutations in receptor tyrosine kinases are almost always absent, at least within the dominant tumor clone, implying that in such tumors activated RAS can completely substitute for tyrosine kinase activity.
Thus, lung adenocarcinomas fall into mutually exclusive molecular subtypes that are associated with mutations involving RAS or various tyrosine kinase genes, an insight that has important implications for targeted therapies in this type of cancer.
這代表一個腫瘤的subclone不會同時有「同一個pathway的上下游genes」突變嗎?
我不太了解為何不能同時有兩種,當上下游同時有genes突變,不會使的這個subclone的生存更有利嗎?
另外這一段似乎也是一樣的概念,但我在Neoplasm的章節就沒有讀懂這背後的意義,所以這一段怎麼讀還是不懂。
Recalling that RAS signal transducers act downstream of receptor tyrosine kinases such as FGFR3, it is not surprising that HRAS and FGFR3 mutations are generally mutually exclusive in bladder cancer.
這是指FGFR3也是receptor tyrosine kinase的一種嗎?
--------------------------------------------
肺腺癌(Lung adenocarcinoma)是怎樣煉成的?
細胞癌化的兩個重要條件:
1. 具有分裂能力的正常細胞。已分化完成的細胞(Terminally differentiated)幾乎不會癌化。
2. 多個DNA突變,或是染色體轉位+DNA突變。癌細胞極少是單一突變造成,單一的染色體轉位也很難使細胞癌化。
造成肺臟上皮細胞DNA突變「主要」的Carcinogen不是吸進去的髒空氣,也不是抽菸的煙霧,而是我們吸進去的O2與細胞膜或細胞周圍的Lipid發生Lipid peroxidation所釋放出來的Free radical對DNA造成傷害。O2與血紅素結合後較不易引發Lipid peroxidation。因此,不抽菸一輩子生活在鄉村呼吸新鮮空氣也會罹患肺腺癌。
EGFR及其下游常發生突變的基因有K-RAS, N-RAS, BRAF, PI3KCA(p110 catalytic subunit)。
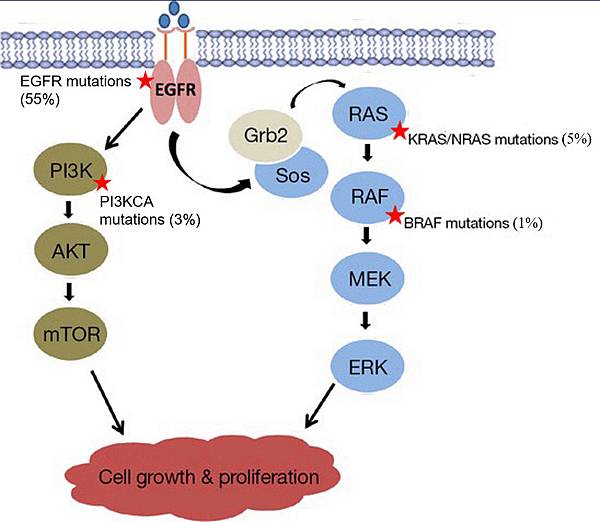
圖一:EGFR及其下游的蛋白在東方人肺腺癌發生突變的頻率。
Receptor tyrosine kinase(RTK)如EGFR突變發生於55%的東方人肺腺癌細胞,但EGFR不會是肺腺癌細胞第一個且/或唯一的突變,因為EGFR activating mutant 會活化下游Oncogenic 及anti-oncogenic (tumor suppressing) signals,在人類細胞,anti-oncogenic signal(p53 stabilization)通常會遠大於Oncogenic signal (ERK)。因此單一的Activating mutation of a receptor tyrosine kinase (EGFR) or its downstream molecules(Ras, Raf, PI3KCA)多半會促使細胞走向死亡,即p53穩定後蛋白量增加--->Check G1 phase and induce apoptosis。如果細胞發生單一的Activating EGFR mutation而沒被p53弄死,則EGFR下游要有Negative feedback(pERK如圖二)抑制太強的Oncogenic signaling,避免p53被刺激出來引導細胞走向死亡。
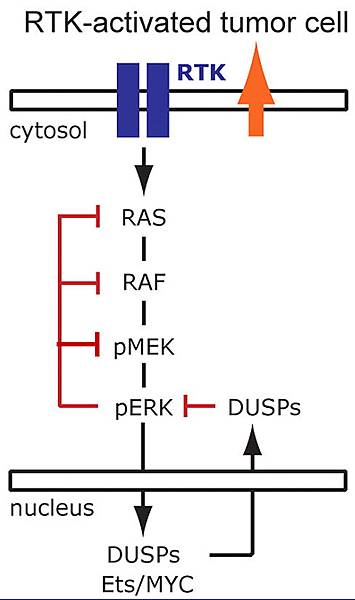
圖二:Negative feedback of RTK signaling by pERK. pERK可抑制RAS, RAF, pMEK, pERK; pERK促進DUSP (dual specificity phosphatase)轉錄, DUSP抑制pERK. ERK=MAP kinase
RTK signaling如何使p53穩定?下面圖三、圖四可說明:

圖三:EGF/EGFR的訊息傳至ERK(-->pERK),Arf mRNA經由E2F/DP1, Myc, Dmp1等Transcription factors被轉錄出來。Arf可抑制Mdm2-mediated p53 ubiquitination,p53因而穩定下來。另一方面,RTK signaling雖然可促使Mdm2基因轉錄(經由pERK--AP1/Ets),但也只是調控Mdm2的量,甚至p53也是Transcription factor可促進Mdm2基因轉錄來調控Mdm2的量,但都無法與Arf抗衡。RTK signaling 因突變而異常活化後的淨結果在上皮細胞是p53穩定,細胞不會因Oncogene activation而癌化,反而是提早走向死亡(p53-mediated apoptosis)。
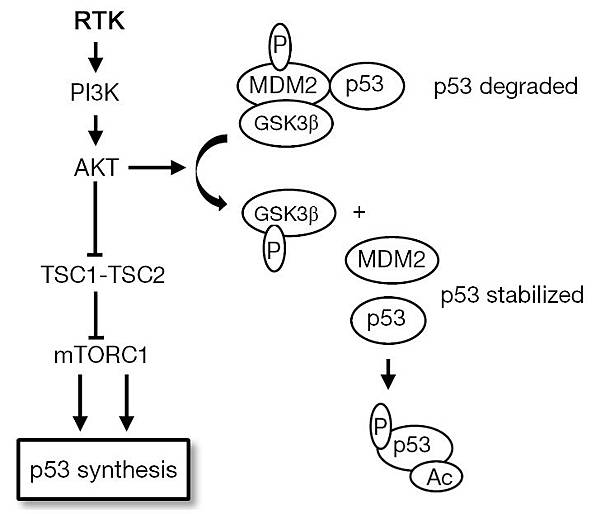
圖四:RTK signaling活化後,p53基因的轉錄可經由Akt/mTORC1提升。Akt將GSK3b磷酸化後,Mdm2與p53會分開,p53經由Phosphorylation及Acetylation而穩定Check G1 phase。
Akt可以把Mdm2磷酸化而強化Mdm2對p53的抑制作用(Ubiquitination/Proteasome degradation),但p53最後會以怎樣的狀態存在,要看何種細胞存在何種刺激下,如果Arf + p53 transcription >> Mdm2,Akt活化後會造成細胞提早死亡,反之,細胞會走向癌化。
上皮細胞癌化最好的選擇是先從抑制p53的Tumor suppressor功能著手,有下列幾種方式:
1. p53突變失去Tumor suppressor功能(即Check G1 phase的功能)。
2. p53 gene promoter被甲基化而無法進行基因轉錄。
3. 基因突變而產生過多的microRNAs or anti-sense RNAs that bind to nascent mRNA of p53,干擾p53 translation。
4. Ink4a/Arf gene deletion or mutation,如此就沒有Arf能抑制Mdm2,p53就無法因Oncogene activation而穩定。Ink4a與Arf是由同一個基因所轉錄的mRNA經不同的Splicing產生兩個不同的蛋白。
一旦p53因突變而失去功能,或無法因Oncogene activation而變穩定(即p53蛋白量增加),那麼由Mutation or chromosome translocation所造成的Ras/MAP kinase signaling 異常活化就無法被制止(MAP kinase activity >>> p53-mediated apoptosis),上皮細胞就會癌化,此時就可能出現 "圖一" 中兩個蛋白同時突變,例如EGFR + K-Ras, K-Ras + BRAF等。
Receptor tyrosine kinase (RTK)有20個Classes: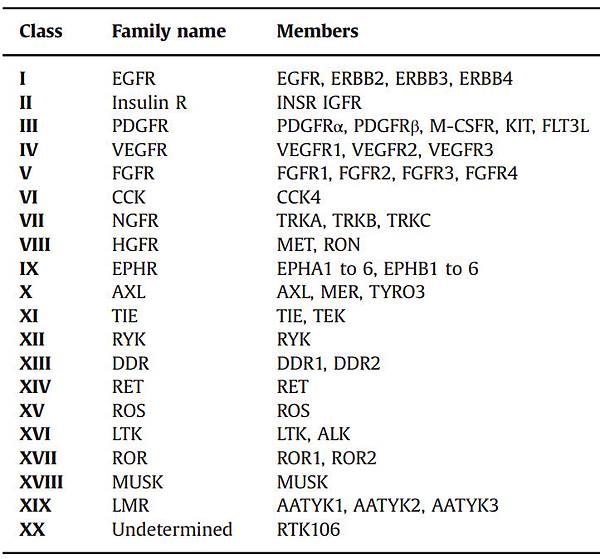

請先 登入 以發表留言。